Мышечная дистрофия, или миопатия, — это группа заболеваний, приводящих к разрушению мышечной ткани, снижению мышечной массы и силы, а также ограничению двигательной активности. Эти состояния могут быть как генетическими, так и приобретёнными. Понимание миопатий важно для диагностики и лечения. В статье рассмотрим основные симптомы миопатий, их влияние на качество жизни пациентов и сосредоточимся на дистрофии Дюшенна, чтобы помочь читателям лучше понять эту патологию и её последствия.
Общие сведения
Что такое миопатия и какие симптомы ее сопровождают? Миопатии, или мышечные дистрофии, представляют собой обширную категорию заболеваний, которые могут быть как генетическими, так и приобретенными. Эти первичные мышечные дистрофии возникают из-за различных нарушений в структуре мышечной ткани и метаболизме, что приводит к постепенному уменьшению мышечной массы, ослаблению мышечной силы и ограничению подвижности (так называемый миопатический синдром).
К основным симптомам миопатий относятся: атрофия мышц (уменьшение объема мышечных волокон и их частичное замещение жировой тканью), быстро прогрессирующая мышечная слабость, снижение мышечного тонуса и рефлексов сухожилий. Миопатии могут передаваться по наследству различными способами: доминантным, аутосомно-рецессивным и сцепленным с полом. Механизмы, лежащие в основе миопатий, связаны с изменениями обменных процессов в мышечных клетках, нарушениями синтеза нуклеиновых кислот и преобладанием процессов распада белков мышечной ткани над их синтезом.
Частота встречаемости мышечных дистрофий аутосомно-рецессивных и аутосомно-доминантных форм в популяции колеблется от 0,9 до 32,6 случаев на 100 тысяч человек. Как уже упоминалось, миопатии охватывают разнообразные группы заболеваний мышечной ткани, клинические проявления которых основываются на миопатическом синдроме. Ниже представлена краткая характеристика некоторых из этих заболеваний.
Врачи отмечают, что миопатия, или мышечная дистрофия, представляет собой группу наследственных заболеваний, характеризующихся прогрессирующей слабостью и атрофией мышц. Специалисты подчеркивают важность ранней диагностики, так как это может существенно повлиять на качество жизни пациентов. Современные методы обследования, включая генетическое тестирование, позволяют выявить заболевание на ранних стадиях. Врачи рекомендуют комплексный подход к лечению, который включает физическую терапию, медикаментозное лечение и, в некоторых случаях, хирургическое вмешательство. Они также акцентируют внимание на необходимости психологической поддержки для пациентов и их семей, так как эмоциональное состояние играет важную роль в процессе адаптации к заболеванию. В целом, мнения специалистов сходятся в том, что своевременное вмешательство и индивидуальный подход к каждому пациенту могут значительно замедлить прогрессирование болезни и улучшить качество жизни.
https://youtube.com/watch?v=ATuRjLpgjeY
Врожденные миопатии
Включает разнообразные заболевания, обусловленные генетическими факторами, которые отличаются по времени появления клинических признаков, локализации мышечных атрофий, скорости прогрессирования и характеру распространения патологических изменений, а также типу наследования. Наиболее тяжелой категорией среди этих заболеваний являются наследственные прогрессирующие мышечные дистрофии (ПМД), которые часто приводят к ранней инвалидности и могут закончиться летальным исходом.
Прогрессирующая мышечная дистрофия. Для этой группы заболеваний характерно поражение определенных мышц при сохранении функции соседних. Наиболее известными являются болезнь Дюшенна и врожденная прогрессирующая миопатия Беккера, которые проявляются в детском возрасте, а также юношеская миопатия Эрба-Рота в различных формах (миопатия Эрба-Рота наследуется по аутосомно-рецессивному типу).
Мышечная дистрофия Дюшенна и миодистрофия Беккера. Эти заболевания связаны с аномалиями на хромосоме X (дистрофин-дефицитные дистрофии). Заболевание затрагивает только мальчиков, так как наследуется по сцепленному с полом (Х) типу. Передача болезни происходит по материнской линии. Частота прогрессирующей миопатии Дюшенна колеблется от 9,7 до 31,0 случаев на 100 000 новорожденных мальчиков.
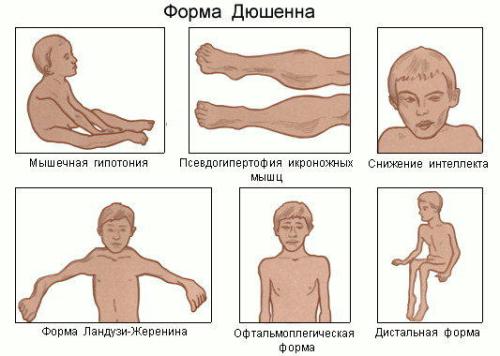
Ферментемия может быть выявлена уже в неонатальный период, однако клинические проявления начинают появляться в возрасте 2-4 лет. Дети с этой патологией начинают поздно ходить, часто падают при попытках бегать, испытывают трудности с прыжками, а из-за слабости проксимальных мышц им сложно подниматься по лестницам или наклонным поверхностям. Из-за контрактуры сухожилий стопы они ходят на больших пальцах. Наблюдается нарастающая псевдогипертрофия икроножных мышц.
У некоторых детей может отмечаться снижение уровня интеллекта. Процесс прогрессирует, и ребенок использует характерные «миопатические» приемы для вставания с пола. К 8-10 годам у них формируется кифосколиоз и гиперлордоз, что значительно нарушает походку. Развивается кардиомиопатия. Обычно к 14-15 годам такие дети становятся обездвиженными, а к 17-20 годам умирают от слабости дыхательной мускулатуры грудной клетки или сердечной недостаточности.
Мышечная дистрофия Беккера имеет более легкое течение по сравнению с миодистрофией. Она начинает проявляться в возрасте 5-15 лет. Характеризуется выраженной слабостью проксимальных мышц ног и тазового пояса. Изменяется походка, возникают трудности при подъеме по лестнице и вставании с низкого стула, также развивается псевдогипертрофия икроножных мышц.
Затем миопатия распространяется на мышцы плечевого пояса и проксимальных отделов рук. Инвалидизация происходит преимущественно на фоне травм или сопутствующих заболеваний.
К наследственным миопатиям относятся: метаболическая миопатия и митохондриальные миопатии. Обычно метаболическая миопатия имеет более легкое течение. Эта относительно медленно прогрессирующая форма характеризуется ранним (обычно с рождения) началом и специфическим симптомокомплексом, известным как синдром «вялого ребенка». Он проявляется мышечной гипотонией, недержанием головы, слабым мышечным сопротивлением, повышенной подвижностью суставов и задержкой в двигательном развитии. Мышечная слабость присутствует с рождения. Дети начинают поздно держать голову, не могут сидеть с прямой спиной, самостоятельно переворачиваться и садиться.
Позже может развиться искривление позвоночника ( кифосколиоз). Митохондриальная миопатия и энцефаломиопатии представляют собой группу заболеваний, вызванных генетическими дефектами в митохондриях (клеточных органеллах, участвующих в тканевом дыхании). В патологический процесс вовлекаются как скелетные мышцы, так и другие органы. Поэтому митохондриальная миопатия характеризуется полиорганными поражениями, включая инсультоподобные эпизоды, эпилептические приступы, нарушения сердечной проводимости, нейросенсорную тугоухость и другие симптомы. Причиной врожденного поражения мышц в виде миопатий и мультисистемных заболеваний могут быть также различные нарушения метаболизма (обмена липидов и гликогена).
| Тип миопатии | Основные симптомы | Возраст начала |
|---|---|---|
| Миопатия Дюшенна | Прогрессирующая мышечная слабость, трудности при ходьбе, падения, увеличение икроножных мышц | Раннее детство (2-5 лет) |
| Миопатия Беккера | Мышечная слабость, аналогичная Дюшенна, но с более медленным прогрессированием | Позднее детство или подростковый возраст |
| Миотоническая дистрофия (тип 1) | Мышечная слабость, миотония (затрудненное расслабление мышц), катаракта, сердечные проблемы | Подростковый или взрослый возраст |
| Фациоскапулогумеральная миопатия (ФСГМ) | Слабость мышц лица, плечевого пояса и рук, асимметричное поражение | Подростковый или взрослый возраст |
| Поясно-конечностная мышечная дистрофия | Слабость мышц тазового и плечевого пояса | Различный, от детства до взрослого возраста |
Приобретённые миопатии
Приобретенные миопатии могут возникать в результате хронических интоксикаций (алкоголизм, токсикомания, наркомания, профессиональные вредности), эндокринных нарушений (болезнь Иценко-Кушинга, гиперпаратиреоз), авитаминозов и мальабсорбции, а также тяжелых хронических заболеваний (сердечная и почечная недостаточность, ХОБЛ, заболевания печени) и опухолевых процессов. Существует несколько категорий:
-
Воспалительные миопатии — это разнообразная группа приобретенных миопатий. К ней относятся такие заболевания, как дерматомиозит, полимиозит и миозит с включениями. Частота заболеваемости колеблется от 0,2 до 0,8 на 100 000 населения, причем среди женщин этот показатель почти в два раза выше, чем среди мужчин. Полимиозит и дерматомиозит проявляются мышечной атрофией и симметричной слабостью, сопровождающейся миалгиями. Без надлежащего лечения существует высокий риск нарушения глотания, а также выраженной слабости мышц шеи и дыхательной мускулатуры. Дерматомиозит обычно развивается остро (в течение нескольких недель), тогда как полимиозит может проявляться от 3-4 недель до нескольких месяцев. Эти заболевания не встречаются у детей и возникают у взрослых старше 20 лет. В то же время миозит с включениями развивается у людей старше 50 лет и имеет постепенное начало. Основной клинический признак — нестабильность коленных суставов, атрофия и слабость мышц бедра, что приводит к частым падениям.
-
Эндокринные миопатии — это вторичные поражения мышц, вызванные нарушениями в работе эндокринных желез. К ним относятся гипертиреоидная и гипотиреоидная миопатии, а также стероидная миопатия. Тиреоидная миопатия развивается на фоне острого тиреотоксикоза и проявляется значительной потерей веса, тремором, гипергидрозом, тахикардией, тревожностью, плаксивостью и бульбарными нарушениями, а также быстро прогрессирующей мышечной слабостью. Миопатия при гипотиреозе характеризуется гипертрофией скелетных и сердечных мышц, отечностью лица, брадикардией, сонливостью, сухостью кожи, ломкостью и тусклостью волос и ногтей, а также судорогами в икроножных мышцах и скованностью.
-
Стероидная миопатия возникает в результате длительного применения кортикостероидов в высоких дозах (в частности, фторсодержащих, таких как Дексаметазон) и проявляется прогрессирующей слабостью в проксимальных мышечных группах, что часто приводит к нарушениям ходьбы.
-
Токсические миопатии развиваются под воздействием токсических веществ (алкогольная, лекарственная и наркотическая миопатия). Острая алкогольная миопатия обычно возникает при длительных запоях у людей, злоупотребляющих алкоголем в течение 15-25 лет. Симптомы развиваются постепенно и проявляются выраженной мышечной слабостью, бульбарными нарушениями, миалгиями, неподвижностью мимики и атрофией мышц.
Важно отметить, что симптомы и методы лечения миопатий могут значительно различаться, поэтому индивидуальный подход к каждому пациенту является крайне важным.
Миопатия, или мышечная дистрофия, вызывает множество обсуждений среди пациентов, их семей и медицинских специалистов. Люди, столкнувшиеся с этой болезнью, часто делятся своими переживаниями о прогрессирующей слабости мышц и ограничениях в повседневной жизни. Многие отмечают, что поддержка близких играет ключевую роль в их эмоциональном состоянии. В социальных сетях можно встретить сообщества, где участники обмениваются советами по адаптации к новым условиям, делятся историями успеха и находят вдохновение в опыте других. Врачи подчеркивают важность ранней диагностики и индивидуального подхода к лечению, что может значительно улучшить качество жизни. Несмотря на трудности, многие люди с миопатией находят способы жить полной жизнью, активно участвуя в реабилитационных программах и поддерживая друг друга.
https://youtube.com/watch?v=rsqWl2tetaQ
Патогенез
Развитие врожденных прогрессирующих миопатий связано с мутациями на Х-хромосоме человека в гене DMD, который отвечает за синтез белка дистрофина. Этот белок является ключевым элементом мышечной ткани и располагается в мембранах скелетных мышечных волокон и кардиомиоцитов.
Дистрофин играет важную роль в обеспечении прочной связи между внеклеточным матриксом и цитоскелетом мышечных волокон. При отсутствии или наличии дефектного дистрофина мышечные волокна становятся уязвимыми, что приводит к их разрыву и увеличению проницаемости мембран во время сокращений. Это, в свою очередь, вызывает выход растворимых ферментов, таких как креатинкиназа, из клеток в обмен на ионы кальция, что активирует фермент фосфолипаза и приводит к дальнейшему увеличению проницаемости мембран. На ранних стадиях заболевания также наблюдается рост уровня активных форм кислорода, что способствует перекисному окислению липидов и повреждению мембран мышечных клеток, а также открытию ионных каналов.
Патоморфологические изменения в основном затрагивают мышцы и проявляются в атрофии отдельных мышечных волокон. В результате миофибриллы теряют свою поперечную сегментацию и могут полностью разрушаться. Ядра мышечных клеток увеличиваются в размерах и содержат различные включения. На месте атрофированных волокон активно разрастается соединительная и жировая ткань. Существенные изменения также наблюдаются в сосудах мышц, где отмечается тенденция к сужению и образованию тромбов. Нервные волокна, в отличие от мышечных, остаются относительно неповрежденными.
Классификация
Существуют различные виды миодистрофий (в сокращении):
https://youtube.com/watch?v=69oly8FNhzU
Прогрессирующие мышечные дистрофии
Х-сцепленные мышечные дистрофии:
- Миодистрофия Дюшенна и Беккера.
- Миодистрофия Эмери-Дрейфуса.
- Дистрофинопатия с синдромом Тернера у девочек.
- Миодистрофия Мэбри.
- Лопаточно-плечевой синдром с деменцией.
- Тазово-бедренная миодистрофия Лейдена-Мебиуса.
- Миодистрофия Роттауфа-Бейера-Мортье.
Аутосомные мышечные дистрофии
- Миодистрофия Ландузи-Дежерина, характеризующаяся лицево-лопаточно-плечевыми нарушениями.
- Миодистрофия Эрба-Рота, проявляющаяся в области конечностей и пояса.
- Миодистрофия Давиденкова, затрагивающая скуловую и плечевую области.
- Миодистрофия Бетлема, отличающаяся специфическими симптомами.
- Окулофарингеальная миодистрофия, влияющая на функции глаз и глотания.
- Окулярная миодистрофия, связанная с нарушениями зрения.
- Дистальные миодистрофии, охватывающие поражения дистальных мышц.
Врожденные миодистрофии
- Врожденная миодистрофия с вовлечением глаз и центральной нервной системы.
- Врожденная миодистрофия с лейкодистрофическими изменениями.
- Цереброокулярная миодистрофия.
Врожденные структурные миопатии (группа заболеваний)
Воспалительные миопатии:
- Полимиозит.
- Острый инфекционный миозит.
- Дерматомиозит.
- Х-сцепленная вакуольная миопатия.
- Миозит с включениями телец.
- Гранулематозный миозит.
Причины возникновения миопатии
Основной причиной врожденной мышечной дистрофии являются генетические нарушения (мутации) в различных генах, что приводит к сбоям в работе митохондрий и ионных каналах миофибрилл, а также нарушает синтез белков и ферментов, ответственных за метаболизм мышечной ткани. Это, в свою очередь, вызывает изменения в структуре мышечных волокон, такие как атрофия и парез мышц, разрастание соединительной ткани и жировое перерождение мышечных волокон, а также инфильтрацию лимфоцитами. Наследование данного заболевания (дефектного гена) может происходить как доминантным, так и рецессивным способом, а также быть связано с полом (Х-хромосомой). Внешние и внутренние факторы, такие как инфекционные болезни (частые ОРЗ, хронический тонзиллит, сальмонеллез, бактериальная пневмония, пиелонефрит и другие), физическое перенапряжение, серьезные травмы, интоксикации различного происхождения и алиментарная дистрофия, часто выступают в роли триггеров, запускающих патологические процессы.
Что касается приобретенных миопатий, то их основными причинами обычно являются эндокринные расстройства (например, болезнь Иценко-Кушинга, гиперпаратиреоз, гиперальдостеронизм), опухолевые процессы, хронические интоксикации (включая профессиональные вредности, токсикоманию, хронический алкоголизм и наркоманию), авитаминозы, мальабсорбция и тяжелые хронические заболевания (такие как ХОБЛ, хроническая почечная недостаточность, хроническая печеночная и сердечная недостаточность).
Симптомы миопатии
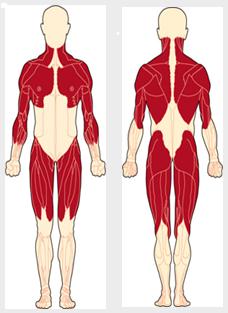
Симптоматика мышечной дистрофии зависит от типа заболевания, скорости его прогрессирования и индивидуальных особенностей пациента. Общими признаками большинства прогрессирующих форм мышечных дистрофий являются выраженная мышечная слабость и атрофия, которые могут проявляться в разные возрастные периоды, но чаще всего — в детском и юношеском возрасте.
У таких детей наблюдается задержка в начале самостоятельной ходьбы, неуклюжесть при передвижении, быстрая утомляемость, трудности при подъеме по лестнице, а также частые падения и спотыкания во время бега. Со временем двигательные нарушения усугубляются, и формируется характерная «утиная» походка. При поражении мышц нижних конечностей и тазового пояса ребенку становится сложно переходить из горизонтального положения в вертикальное; если вовлечены дистальные группы мышц ног, развивается «петушиная» походка. Обычно наличие таких симптомов и их прогрессирование позволяют диагностировать миодистрофию на ранних стадиях. При обследовании таких детей на начальных этапах заболевания выявляется локальная атрофия мышц, которая со временем становится генерализованной.
Атрофированные мышцы при пальпации выглядят дряблыми и истонченными, однако в некоторых случаях (например, при миопатии Дюшенна) наблюдается псевдогипертрофия, когда атрофированные мышцы замещаются соединительной или жировой тканью. Процесс миодистрофии сопровождается миосклерозом, поражением соединительной ткани, развитием сухожильно-связочных ретракций, укорочением ахиллова сухожилия, ограничением подвижности в суставах и даже контрактурами. Параллельно с развитием мышечных атрофий заметно снижаются сухожильные рефлексы, такие как коленные.
При вовлечении мышц плечевого пояса возникают ограничения в движениях плечевых суставов. Такие пациенты не могут поднять руки выше горизонтального уровня, в то время как подвижность в локтевых и лучезапястных суставах, а также сила мышц сохраняются на протяжении длительного времени.
Среди симптомов можно выделить «свободные надплечья» (при подъеме пациента за подмышки его голова проваливается в плечи) и «крыловидные лопатки» (лопатки отстают от туловища). При поражении мышц тазового дна у больного возникают трудности при вставании из сидячего положения и подъеме по лестнице. В таких случаях пациенту приходится опираться на посторонние предметы или подниматься «лесенкой» (поэтапно).
Изменяется походка, она становится раскачивающейся и переваливающейся (утиная походка). Слабость длинных мышц спины приводит к нарушению осанки, выпячиванию живота и искривлению позвоночника. При атрофии косых мышц живота формируется «осиная» талия. На стадии выраженных нарушений (отсутствие движений из-за атрофии мышц) могут возникать контрактуры, что приводит к невозможности движения в суставах или их тугоподвижности.
Как правило, атрофия мышц ног и стоп сопровождается их слабостью, что формирует характерную «петушиную» походку (больные вынуждены поднимать голень высоко). При атрофии и слабости лицевых мышц (плечелопаточно-лицевая форма Ландузи—Дежерина) наблюдается симптом «полированного лба» (отсутствие морщин на лбу), а также гипомимия — пациенты не могут надуть щеки, плотно зажмурить глаза или вытянуть губы в трубочку. При замещении мышц губ соединительной или жировой тканью они значительно утолщаются.
При поражении наружных глазных мышц (офтальмоплегическая мышечная дистрофия) наблюдается миопатия глаз. Основные симптомы этой миопатии включают птоз и ограничение подвижности глазных яблок, вплоть до их полной неподвижности. Если в процесс вовлечены мышцы глотки и гортани, у пациента развивается осиплость голоса и возникают проблемы с глотанием. На фоне метаболической миопатии может развиться нетравматический рабдомиолиз, который приводит к острой почечной недостаточности.
Рабдомиолиз возникает из-за массивного поражения поперечнополосатых мышечных волокон и сопровождается появлением свободного миоглобулина в крови. Симптомы рабдомиолиза зависят от степени миоглобинурии и сопутствующих нарушений. Типичные проявления включают общую слабость, резкую мышечную слабость, боли в мышцах, тошноту и тяжесть в пояснице. Рабдомиолиз может сопровождаться анурией, а моча окрашивается в темно-бурый цвет. В дальнейшем развиваются симптомы острой почечной недостаточности.
Врожденная миопатия у детей часто сопровождается нарушениями вентиляционной функции легких, которые в большинстве случаев обусловлены внелегочными причинами, такими как патология опорно-двигательного аппарата (деформация позвоночника, туловища). Сопутствующая кардиальная патология (кардиопатии, миокардиодистрофии) приводит к нарушениям кровообращения в малом круге, что ухудшает микроциркуляцию в легких и постепенно вызывает явную или скрытую хроническую дыхательную недостаточность.
Большинство форм прогрессирующих мышечных дистрофий не сопровождаются снижением интеллекта, реже наблюдаются выраженные эмоциональные нарушения (замкнутость, повышенная раздражительность, подавленное настроение). В целом, пациенты критически относятся к своему состоянию и большинство из них успешно обучаются в учебных заведениях.
При прогрессирующих миопатиях значительную часть клинических проявлений составляют ортопедические проблемы, среди которых наиболее часто встречаются деформации позвоночника, туловища и конечностей; вывихи и подвывихи тазобедренных суставов, деформация стоп, нестабильность надколенника, гипермобильность суставов, сухожильные ретракции, а также контрактуры мышц и суставов.
Клинические особенности некоторых форм миопатий
Болезнь Дюшенна
Мышечная дистрофия Дюшенна считается самой тяжелой и распространенной формой прогрессирующих миопатий, согласно данным Википедии. Эта болезнь проявляется в раннем возрасте, обычно между 2 и 3 годами, и характеризуется стремительным развитием слабости проксимальных мышц, сначала в нижних, а затем и в верхних конечностях.
Дети, страдающие этой формой дистрофии, часто ходят с раскачивающейся походкой, на пальцах ног, и у них наблюдается выраженный лордоз. Им трудно вставать с пола, прыгать, бегать и подниматься по лестнице. Частые падения приводят к переломам рук или ног почти у 20% таких детей. Слабость мышц прогрессирует стабильно, и практически у всех пациентов развивается сколиоз, а также сгибательные контрактуры конечностей и заметная псевдогипертрофия, когда жировая или соединительная ткань замещает отдельные группы мышц.
Одной из характерных черт дистрофии Дюшенна является вовлечение сердечной мышцы в патологический процесс, что происходит в 90% случаев. Это может привести к развитию дилатационной кардиомиопатии, сопровождающейся нарушениями проводимости, а иногда и аритмией.
Еще одной особенностью является легкое непрогрессирующее слабоумие, которое затрагивает вербальные навыки и вызывает различные нейроповеденческие расстройства, такие как синдром гиперактивности и дефицита внимания, расстройства аутистического спектра и проблемы с когнитивными функциями. Это затрудняет процесс обучения для ребенка. К сожалению, большинство таких детей становятся зависимыми от инвалидных колясок и, как правило, умирают от осложнений к 20 годам.
Прогрессирующая миодистрофия Беккера
По клиническим проявлениям данное заболевание во многом схоже с формой Дюшенна, однако его течение более благоприятное. Оно проявляется позже, в возрасте 10-15 лет, и протекает мягко, позволяя пациентам сохранять работоспособность на протяжении длительного времени; в 20-30 лет, а иногда и позже, они могут продолжать ходить.
Фертильность не нарушена, что приводит к тому, что заболевание может наблюдаться в 2-3 поколениях (так называемый «эффект деда») — мужчина, страдающий этим недугом, передает его через свою дочь внуку. Прогрессирование болезни происходит медленно. Реакция ахилловых сухожилий выражена менее резко. Сердечно-сосудистые нарушения отсутствуют или проявляются умеренно (например, кардиалгии, блокада ножек пучка Гиса). Уровень интеллекта остается на нормальном уровне.
Плечелопаточно-лицевая форма миопатии Ландузи—Дежерина
Заболевание проявляется в возрасте от 10 до 20 лет. Атрофия и мышечная слабость затрагивают мимические мышцы лица, а также плечевой пояс и лопатки. Лицо становится менее выразительным: губы становятся толстыми и вывернутыми, лоб приобретает «полированный» вид, а улыбка становится «поперечной». Атрофия мышц плеча и трапециевидной мышцы приводит к появлению характерных признаков, таких как «крыловидные» лопатки, симптом свободных надплечий, сколиоз и уплощение грудной клетки. На ранних стадиях заболевания мышечный тонус снижен, в основном, в проксимальных группах мышц. Болезнь развивается медленно, и работоспособность сохраняется на длительное время.
Окулофарингеальная миопатия
Отмечается одновременное поражение глазодвигательных мышц, сопровождающееся заметной слабостью мышц глотки и языка. Уникальной чертой является позднее начало заболевания, которое проявляется в возрасте 40-60 лет. Первоначально наблюдается двусторонний птоз, за которым следует ухудшение функции глотания.
Анализы и диагностика
Диагностика «мышечной дистрофии» осуществляется на основании следующих факторов:
- Присутствия характерных клинических симптомов.
- Результатов ДНК-исследования (обнаружение мутаций в генах).
- Данных биопсии нервно-мышечного лоскута (выявление специфических дистрофических изменений в мышечной ткани).
- Уровня креатинфосфокиназы (КФК) в плазме крови — значительное увеличение показателя.
- Результатов магнитно-резонансной томографии мышц (наличие соединительнотканных или жировых изменений в мышцах).
Дифференциальная диагностика проводится с учетом других нервно-мышечных заболеваний различного происхождения, таких как невральные и спинальные мышечные атрофии, травмы мышц и нервов, наследственные болезни, связанные с поражением двигательных нейронов спинного мозга, а также воспалительные заболевания мышц.
Лечение миопатии
На сегодняшний день не существует специфического лечения мышечной дистрофии. Главная цель терапии заключается в том, чтобы максимально продлить период, когда пациент может передвигаться самостоятельно. При длительном нахождении в лежачем положении у больных быстро развиваются такие осложнения, как сколиоз, контрактуры и нарушения дыхания. Лечебный комплекс включает в себя медикаментозную терапию, массаж, лечебную физкультуру и ортопедические мероприятия. Основой медикаментозного лечения является симптоматическая терапия, направленная на замедление прогрессирования миопатий и поддержание функционирования жизненно важных органов и систем организма.
Для замедления дистрофических процессов применяются глюкокортикоиды, такие как преднизолон в дозировке 5 мг в таблетках (0,75 мг/кг/сутки) курсами по два месяца с перерывами в 2-3 месяца. Оксазолон (дефлазакорт) рекомендуется пациентам с предрасположенностью к ожирению.
При легкой и средней степени тяжести заболевания, когда наблюдается стойкая компенсация, целесообразно назначение препаратов с выраженным метаболическим действием. Эти средства помогают поддерживать и нормализовать обменные процессы, а также улучшают энергетические процессы в кардиомиоцитах и неповрежденных миоцитах. К таким препаратам относятся Элькар (левокарнитин), АТФ-лонг, метионин, цитофлавин, тиоцетам, пирацетам, кардонат, милдронат, магнерот, рибоксин, витамины Е и А, а также никотиновая кислота. Их назначают курсами по 1-2 препарата 2-3 раза в год. При выраженных болях и ощущении «стягивания» в мышцах нижних конечностей хорошо зарекомендовал себя цитруллин малат, который способствует «утилизации» молочной кислоты благодаря своим метаболическим свойствам.
На стадии субкомпенсации при доброкачественных формах, а также на стадии компенсации при быстро прогрессирующих формах ПМД (Дюшенна, Эрба-Рота) на ранних этапах заболевания назначается раствор карнитина хлорида, обладающий выраженными метаболическими, кардиотрофическими, нейротрофическими и антиоксидантными свойствами. Его применяют совместно с аскорбиновой кислотой и кокарбоксилазой на фоне перорального приема метионина и внутримышечного введения пиридоксина гидрохлорида (3-4 курса в год по 10 инъекций). Также при этих формах назначаются антигомотоксические препараты, такие как предуктал МВ (триметазидин), а также средства с нейротрофическим действием (траумель, церебрум композитум).
На стадии выраженной клинической картины при миодистрофии Дюшенна назначается иммуноглобулин человека в дозе 5,0-7,0 мл/кг на инфузию. Использование иммуноглобулина способствует увеличению силы и улучшению переносимости физических нагрузок. Для стимуляции процессов регенерации тканей назначается раствор актовегина. Проводится метаболическая терапия, направленная на улучшение обмена веществ в костной ткани, скелетных мышцах, клетках миокарда и печени, а также на нормализацию жирового обмена. Витамины группы В (цианокобаламин и тиамин-хлорид), препараты кальция, витамин D3 и левокарнитин также широко применяются. Кроме того, используются антихолинэстеразные препараты пролонгированного действия, такие как нивалин, нейромидин, прозерин, оксазил и галантамин.
При наличии когнитивных нарушений (при ПМД Дюшенна) наряду с традиционными ноотропными средствами (луцетам, церебролизин, тиоцетам и др.) эффективно назначается семакс, который чередуется с приемом когитума и цераксона.
Лечение ортопедических проявлений
При первых признаках контрактур и сокращения сухожилий рекомендуется проводить мягкий массаж с использованием фармакопунктуры с препаратом Траумель С и трофическими мазями, которые способствуют улучшению питания суставов. Также необходимо зафиксировать конечность в том положении, которое было достигнуто в результате коррекции суставной контрактуры, а на ночь фиксировать конечности в физиологически правильном положении. Для облегчения передвижения пациента используются ортопедические стельки, специальная обувь и наколенники.
Для укрепления и поддержания мышечного корсета назначается паравертебральная фармакопунктура с такими препаратами, как актовегин, нейромидин, церебролизин, кортексин и цианокобаламин. На стадии субкомпенсации, особенно во время значительных нагрузок на позвоночник (например, при ходьбе или сидении), рекомендуется носить реклинаторы и корсеты в течение 2-4 часов. При тяжелой декомпенсации показано постоянное использование корсетов. В случае развития остеопороза целесообразно назначение препаратов, содержащих кальций, таких как Кальцемин Адванс.
Терапия приобретенных форм миопатий
Лечение основного заболевания включает в себя несколько ключевых аспектов: детоксикацию организма и устранение токсического воздействия, подавление инфекционного процесса, коррекцию эндокринных нарушений и заболеваний, а также перевод хронической формы болезни в стадию устойчивой ремиссии и другие меры.
Психологическая готовность как родителей, так и ребенка играет важную роль в процессе лечения. Рекомендуется, чтобы родители прошли курс семейной психотерапии, а детям — индивидуальную. Важно, чтобы родители не замыкались на своих проблемах, а активно взаимодействовали с другими семьями, сталкивающимися с аналогичными трудностями. Это можно сделать через интернет-ресурсы, такие как форумы и порталы, посвященные миопатии. Также стоит регулярно следить за новыми данными о перспективных методах лечения и актуальными новостями в этой области медицины на сайте «миопатия ру».
Лекарства
Преднизолон, Пирацетам, Метионин, Колекальциферол, Луцетам, Рибоксин, Цианокобаламин.
Процедуры и операции
Существует множество методов физиотерапии, среди которых можно выделить парафиновые и грязевые аппликации, электростимуляцию мышц, ультразвуковую терапию, а также электрофорез с использованием нейромидина, неостигмина, прозерина и никотиновой кислоты. Также применяются ионофорез с кальцием, легкий массаж и лечебная физкультура (ЛФК). Особое внимание уделяется регулярным занятиям лечебной гимнастикой, которая включает как пассивные, так и активные движения в различных положениях и во всех суставах. Активные движения рекомендуется выполнять в изометрическом режиме. Важно помнить о необходимости избегать чрезмерных нагрузок и особенно упражнений, которые могут привести к перерастяжению мышц. Не менее значимыми являются дыхательные упражнения, особенно в случаях, когда пациент находится в состоянии иммобилизации.
При наличии показаний могут проводиться ортопедические операции, такие как удлинение ахиллова сухожилия, коррекция деформации стопы, рассечение фасций и пластика суставов.
Диета
Специально разработанная диета для людей с врожденными прогрессирующими миопатиями не существует, однако есть ряд рекомендаций, которые могут помочь улучшить состояние пациента. Основой питания должна стать сбалансированная диета, богатая животным белком (включая диетические сорта мяса, рыбу, морепродукты, творог и куриные яйца), с ограничением животных жиров и достаточным количеством растительных масел, цельнозерновых продуктов, свежих овощей и фруктов. Это обеспечит организм необходимыми природными антиоксидантами, токоферолами, аскорбиновой кислотой, каротиноидами и другими веществами, которые способствуют укреплению антиоксидантной защиты. В дополнение к основным продуктам в рацион стоит включить:
- Продукты, богатые селеном. Исследования показывают, что у пациентов с прогрессирующей мышечной дистрофией уровень селена в сыворотке крови снижен. Селен обладает мощными антиоксидантными свойствами и влияет на уровень свободных радикалов и пероксидов липидов. Источниками селена являются морепродукты, чеснок, грибы, зародыши пшеницы, цельные зерна, пивные дрожжи, куриное мясо, бурый рис, красные водоросли, брокколи, лук и лосось.
- Таурин. Эта аминокислота необходима для нормального обмена кальция, натрия, калия и магния. Она способствует повышению внутриклеточной концентрации калия и улучшает проводимость клеточных мембран. Таурин содержится в птице, яйцах, рыбе, моллюсках и мясе.
- Кофермент Q10. Является важным кофактором для митохондриального дыхания и антиоксидантом, обладающим мембраностабилизирующим эффектом. Наибольшее количество кофермента Q10 можно найти в печени, мясе, бычьем сердце, сардине, макрели, лососе, арахисе и шпинате.
- Зеленый чай. Исследования на животных показали, что регулярное употребление зеленого чая может уменьшить мышечную слабость у лабораторных животных. Таким образом, зеленый чай (в количестве 5-7 чашек в день) может иметь терапевтический потенциал для предотвращения атрофии миоцитов. Ученые пришли к выводу, что при наследственных мышечных дистрофиях полезно употреблять зеленый чай как антиоксидант и ловушку свободных радикалов, что способствует снижению окислительного стресса в скелетной и сердечной мускулатуре.
Для поддержания необходимого уровня минералов в организме рекомендуется включать в рацион чаи из монотрав или смеси нескольких трав, настаиваемых 10–20 минут из корней и 5–10 минут из цветков или листьев, с употреблением 2–3 чашек в день. При прогрессирующей мышечной дистрофии полезны чаи из следующих трав:
- Для минерализации рациона — хвощ полевой, крапива двудомная, овес посевной, пырей ползучий.
- При мышечной слабости и миалгии: таволга вязолистная, писцидия ярко-красная.
Профилактика
Профилактика наследственных миопатий включает в себя внимательный сбор семейной истории, особенно у пар, в которых есть родственники с диагнозом наследственной миопатии. Таким семьям рекомендуется пройти медико-генетическую консультацию, желательно на этапе планирования беременности, чтобы оценить вероятность рождения ребенка с миопатией.
На сегодняшний день мышечная дистрофия Дюшенна может быть выявлена еще до рождения. Для этого необходимо провести анализ амниотической жидкости и клеток плода на наличие мутации. Обнаружение такой мутации может стать основанием для обсуждения вопроса о возможности рождения ребенка, однако решение принимается врачами медико-генетической консультации совместно с родителями в каждом конкретном случае.
Ключевым аспектом профилактики приобретенных форм миопатий является своевременное лечение эндокринных и инфекционных заболеваний, а также предотвращение воздействия токсических веществ на организм и коррекция метаболических нарушений.
Последствия и осложнения
Врожденные прогрессирующие миопатии часто связаны с повышенным риском возникновения следующих осложнений:
- Искривления позвоночника.
- Проблем с сердечной функцией.
- Потери двигательной активности и последующей инвалидизации.
- Заболеваний органов дыхания, которые могут привести к дыхательной недостаточности.
- Нарушений когнитивных функций, памяти и способности к обучению.
- Ранней смерти.
Прогноз
Прогноз при наследственных врожденных миопатиях в целом считается неблагоприятным, однако он во многом зависит от типа миопатии, степени тяжести, скорости прогрессирования и уровня дистрофии скелетных мышц, а также от вовлеченности дыхательных и сердечных мышц в патологический процесс. Наиболее тяжелый прогноз наблюдается при мышечной дистрофии Дюшенна, когда пациенты, как правило, не доживают до 20-25 лет. В то же время, поздние формы миопатий, проявляющиеся после 20-30 лет, имеют более благоприятное течение и менее агрессивный характер.
Пациенты могут вести относительно нормальный образ жизни и даже выбрать профессию, соответствующую их физическим возможностям, в зависимости от степени поражения мышц (например, ручной или умственный труд). Тем не менее, даже при других типах миопатий риск инвалидизации остается высоким. Прогноз для приобретенных миопатий, при условии успешного лечения основного заболевания, которое вызвало миопатию, более оптимистичен.
Список источников
- Гринио Л.П., Агафонов Б.В. Миопатии. — Москва: Медицина, 1997. — 213 страниц.
- Казаков В.М. Клинико-молекулярно-генетическая классификация мышечных дистрофий (научный обзор с комментариями) // Неврологический журнал. — 2001. — Вып. 3. — С. 47-52.
- Дадали E.О., Мальмберг С.А., Подагова Е.В., Поляков A.B., Петрухин A.C. Особенности клинических проявлений прогрессирующей мышечной дистрофии Дюшенна у гетерозиготных носительниц мутации в гене дистрофина // Российский медицинский журнал. — 2007. — Вып. 3. — С. 18-21.
- Шаймурзин М.Р., Евтушенко С.К. Новейшие технологии в терапии нервно-мышечных заболеваний, направленные на замедление их прогрессирования // Вестник физиотерапии и курортологии. — 2010. — Вып. 6. — С. 40-41.
- Шишкин С.С., Шаховская Н.И., Крахмалева И.Н. Клинический полиморфизм, генетическая гетерогенность и проблемы патогенеза первичных миопатий // Журнал неврологии и психиатрии. — 2002. — Вып. 2. — С. 54-60.
Современные исследования и перспективы лечения
Современные исследования в области миопатий и мышечной дистрофии активно развиваются, что связано с необходимостью поиска эффективных методов лечения и улучшения качества жизни пациентов. Научные работы охватывают широкий спектр направлений, включая генетические исследования, клеточную терапию, генные технологии и фармакологические подходы.
Одним из наиболее перспективных направлений является генотерапия, которая нацелена на исправление генетических дефектов, вызывающих миопатию. Исследования показывают, что использование векторов, таких как аденоассоциированные вирусы (AAV), позволяет доставлять исправленные гены непосредственно в мышечные клетки. Это может привести к восстановлению функции мышц и замедлению прогрессирования заболевания. В клинических испытаниях уже наблюдаются обнадеживающие результаты, особенно в отношении дистрофии Дюшенна.
Клеточная терапия также представляет собой многообещающий подход. Исследователи изучают возможность использования стволовых клеток для регенерации поврежденных мышечных тканей. Применение мезенхимальных стволовых клеток, полученных из жировой ткани или костного мозга, продемонстрировало способность к дифференцировке в мышечные клетки и улучшению функциональных показателей у животных. Однако, несмотря на многообещающие результаты, необходимы дополнительные исследования для оценки безопасности и эффективности этого метода у людей.
Фармакологические подходы также продолжают развиваться. В последние годы внимание исследователей привлекли препараты, направленные на улучшение метаболизма мышц и уменьшение воспалительных процессов. Например, использование кортикостероидов может замедлить прогрессирование некоторых форм миопатий, однако долгосрочное применение этих препаратов связано с серьезными побочными эффектами. Поэтому активно исследуются альтернативные препараты, такие как модуляторы миостатинов, которые могут способствовать росту мышечной массы и улучшению силы.
Кроме того, важным аспектом современных исследований является разработка методов ранней диагностики миопатий. Генетические тесты и молекулярно-генетические исследования позволяют выявлять предрасположенность к заболеваниям на ранних стадиях, что открывает новые горизонты для профилактики и лечения. Раннее вмешательство может значительно улучшить прогноз и качество жизни пациентов.
В заключение, современные исследования в области миопатий и мышечной дистрофии открывают новые горизонты для лечения и управления этими заболеваниями. Несмотря на существующие вызовы, такие как сложность генетических механизмов и необходимость в долгосрочных клинических испытаниях, достижения науки и медицины вселяют надежду на создание эффективных терапий, которые смогут изменить жизнь миллионов людей, страдающих от этих заболеваний.
Вопрос-ответ
Можно ли вылечить дистрофию мышц?
Лечение мышечной дистрофии Дюшена: к сожалению, данное заболевание является неизлечимым.
Что такое миопатия при мышечной дистрофии?
Мышечные дистрофии и миопатии — это заболевания, при которых мышцы со временем ослабевают и уменьшаются в размерах. По мере ослабления мышц становится труднее двигаться и выполнять повседневные действия.
Что такое дистрофия Миоши?
Миопатия Миоши (ММ) — одна из редких дистальных форм поясно-конечностных мышечных дистрофий, характеризуется слабостью, первоначально затрагивающей икроножные мышцы в подростковом или раннем взрослом возрасте, медленно прогрессирующим течением, «восходящим» паттерном вовлечения мышечных групп в атрофический процесс.
Советы
СОВЕТ №1
Регулярно консультируйтесь с врачом-неврологом или специалистом по миопатиям для своевременной диагностики и корректировки лечения. Это поможет вам лучше понять свое состояние и получить индивидуальные рекомендации по терапии.
СОВЕТ №2
Поддерживайте активный образ жизни в рамках своих возможностей. Физическая активность, такая как легкие упражнения или физиотерапия, может помочь сохранить мышечную силу и улучшить общее состояние здоровья.
СОВЕТ №3
Обратите внимание на питание. Сбалансированная диета, богатая витаминами и минералами, может поддержать здоровье мышц и общее самочувствие. Рассмотрите возможность консультации с диетологом для составления подходящего рациона.
СОВЕТ №4
Присоединяйтесь к группам поддержки или сообществам людей с миопатией. Общение с теми, кто сталкивается с похожими проблемами, может помочь вам получить эмоциональную поддержку и полезные советы по управлению заболеванием.